बोर का पूरा नाम था- नील्स हेनरिक डेविड बोर। इनका जन्म 1885 को डेनमार्क में हुआ। सन् 1913 में बोर द्वारा परमाणु मॉडल पेश किया गया।
नील्स बोर द्वारा रदरफोर्ड के परमाणु मॉडल में कुछ तथ्यों की अनुपस्थिति का अंदाजा लगाया गया तथा प्लांक के क्वाण्टम सिद्धांत की सहायता लेते हुए बोर ने अपना एक मॉडल तैयार किया।
यह मॉडल नील्स बोर द्वारा परमाणु के सम्बन्ध में पेश किया गया था।
इसे रदरफोर्ड-बोर मॉडल भी कहा जाता है, क्योंकि यह रदरफोर्ड के परमाणु मॉडल में कुछ स्थितियों में सुधार व नवीनीकरण करके बनाया गया था, अतः काफी हद तक रदरफोर्ड के मॉडल से मेल खाता हुआ था।
बोर के इस मॉडल के अनुसार यह बात प्रस्तुत की गयी थी कि इलेक्ट्रॉन द्वारा नाभिक के बाहरी ओर निरन्तर तेज गति से चक्कर लगाये जाते हैं। इसके लिए इलेक्ट्रॉन को ऊर्जा या बल की आवश्यकता पड़ती है। इसे अपकेंद्रिय बल कहते हैं।
जब विद्युत के ऋण आवेश युक्त इलेक्ट्रॉन का नाभिक के चक्कर लगाने से इसमें स्थित धन आवेश वाले प्रोटॉन के कारण इनके मध्य आकर्षण बल उत्पन्न होता है। यह आकर्षण बल ही इलेक्ट्रॉन को अपकेंद्रिय बल देने में सहायक होता है। इसके कारण ही इनमे गति करने की ऊर्जा बनी रहती है।
अतः बोर के परमाणु मॉडल के परिणामस्वरूप यह बात स्पष्ट होती है कि इलेक्ट्रॉन को अपकेंद्रिय बल नाभिक में स्थित प्रोटॉन के होने से प्राप्त होता है।
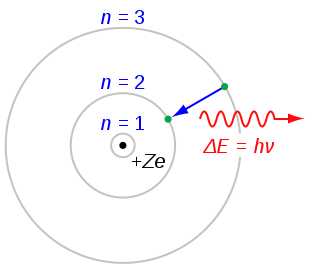
बोर ने अपने मॉडल में इस बात का भी व्याख्यान किया कि परमाणु के भीतर स्थित नाभिक के बाहृ भाग में भिन्न-भिन्न स्तर (कक्षा या कक्ष) सृजित हुए होते हैं, जिनमे इलेक्ट्रॉन वृत्ताकार गति करते हैं।
इन भिन्न-भिन्न स्तरों पर ऊर्जा का स्तर भी भिन्न होता है अर्थात् जो स्तर या कक्ष नाभिक के अधिक नज़दीक होगा, उसमे ऊर्जा काफी कम होगी। जैसे-जैसे इन कक्षों की स्थिति नाभिक से दूर होती जाती है, वैसे-वैसे इनमे ऊर्जा का स्तर बढ़ता जाता है।
परमाणु में किसी कारणवश यदि ऊर्जा में परिवर्तन होता है, तो इलेक्ट्रॉन द्वारा भी कक्षों या ऊर्जा स्तरों में परिवर्तन होने लगता है।
जब परमाणु के भीतर इलेक्ट्रॉन अपने एक ही कक्ष में स्थायी रूप से गतिमान रहता है तो इसे आद्य अवस्था कहा जाता है।
जब ऊर्जा स्तर में बदलाव के कारण इलेक्ट्रॉन एक कक्ष की त्यागकर दूसरे कक्ष में पहुँच जाता है तो इसे इलेक्ट्रॉन की उत्तेजित अवस्था कहा जाता है।
इलेक्ट्रॉन द्वारा गति करते वक्त इन कक्षों के कारण ऊर्जा का निर्धारण होता है, जिससे इलेक्ट्रॉन में तीव्रता पैदा होती है। इसी वजह से विकिरण को उत्सर्जित नही कर पाते।
इस बिंदु ने रदरफोर्ड के मॉडल की कमी को दूर कर दिया, क्योंकि यहाँ यह बात सिद्ध हुई कि विकिरण का उत्सर्जन न होने के कारण इलेक्ट्रॉन नाभिक के भीतर नही गिर सकते।
कमियाँ- परमाणु में इलेक्ट्रॉन द्वारा गतिशील रहने के दौरान उनमे पाई जाने वाली ऊर्जा का स्तर कम व ज्यादा होता है। इससे इलेक्ट्रॉन द्वारा अपने कक्षों में भी परिवर्तन किया जाता है। इस कारण स्पेक्ट्रम रेखाओं का सृजन होता है।
चुम्बकीय प्रभाव वाले क्षेत्र में इन स्पेक्ट्रम रेखाओं में विभाजन होता है, इससे पड़ने वाला प्रभाव “ज़ीमान प्रभाव” कहलाता है।
विद्युत प्रभावी क्षेत्र में स्पेक्ट्रम रेखाओं में विभाजन होने की क्रिया से पड़ने वाले प्रभाव को “स्टॉर्क प्रभाव” कहते हैं।
बोर द्वारा प्रस्तुत किये गए मॉडल में ज़ीमान प्रभाव व स्टॉर्क प्रभाव दोनों का स्पष्टीकरण नही किया गया।
निष्कर्ष- बोर द्वारा अपना परमाणु मॉडल प्रस्तुत होने से पहले ही परमाणु की संरचना के सम्बन्ध में बहुत से तथ्य साबित हो चुके थे, जैसे- परमाणु का विभाजन नही किया जा सकता, परमाणु के केन्द्र में नाभिक(केन्द्रक) पाया जाता है व परमाणु कई छोटे-छोटे कणों से मिलकर बनता है। इनमे से कुछ धनावेशित, ऋणावेशित व उदासीन प्रकृति के होते हैं।
बोर द्वारा रदरफोर्ड के मॉडल को उच्च स्तर पर ले जाकर उसमे नई खोजों के तथ्यों को जोड़ा गया व परमाणु सरंचना सम्बन्धी कुछ नियमों से ज्ञात करवाया गया। कुछ कमियों के अलावा बोर का मॉडल काफी कामयाब रहा।

this is useful for me
नील्स बोर कक्षाओं का नाम के K L M N क्यों रखा
K l m n kyo rakha gaya
K l m n nam kyu rakha
This is useful for me
Thanks
Nice information about that scientist
Tysm ji
Very nice
good …………….
sir this is useful for me and my friends